はじめに
急性期の輸液管理はICUに限らず病棟管理では必須とも言える能力ですが、様々な要素が関わっており、一概に評価することは難しい、、、
それでも、基本的なことを分かっているか、分かっていないか、で診療の質に差が出てくる部分なので、しっかり抑えておきたいところです。
輸液の目的
輸液の目的は、主に以下の5つに分類されます。
①Resuscitation fluid:蘇生や急性期治療のために行われるもの
②Maintenance fluid:尿、排便、不感蒸泄など、生理的に失われた水分や電解質の補充のために行われるもの
③Replacement fluid:嘔吐、下痢、ドレーン廃液など、生理的なもの以外で失われた水分や電解質の補充のために行われるもの
④Nutrition fluid:栄養補充のために行われるもの
⑤Fluid creep:ラインキープや抗菌薬の溶媒などのために投与されるもの
(Intensive Care Med. 2018; 44: 409-17.) (PMID 30335338)
何を目的にした輸液なのかを把握することはとても重要です。
重症症例ではReuscitation fluidで輸液を必要とすることが多く、やがて補充した輸液が戻ってくるので多くはMaintenance fluid、いわゆる維持輸液はあまり必要になりません。
Resuscitation fluidの目的
Resuscitation fluidの目的は、ショックを是正することです。
詳しくは別記事(また後日記載します)を参照頂ければと思いますが、ショックとは末梢組織での酸素需要と酸素供給のバランスが壊れたものです。大事なのは①酸素運搬が大丈夫か?②組織灌流ができているか?の2つが着眼点としてあり、それぞれ基準となる式があります。
①酸素運搬:DO2 ≒ 1.34 × Hb × SaO2 × CO
(※DO2:Delivery O2、酸素供給量 CO:心拍出量)
②組織灌流:MAP – CVP = CO × SVR
(※MAP:平均血圧、CVP:中心静脈圧、SVR:体血管抵抗)
こうしてみるといずれの式にもCO(心拍出量)が関わっていませんか?
急性期輸液の目的は、ショックを改善させることにありますが、突き詰めると「COを改善させる」ことにあります。さらにいえば
CO = SV × HR (※SV:一回拍出量 , HR:心拍数)
であり、輸液では直接的にHRを変化させることはできないので(代償性変化で変えることはできますが)、
「究極的にはResuscitation fluidの目的はSVを改善してショックを是正すること」
にあるといえます。
輸液の原則
鉄則その1:なんのための輸液なのか目的を明確にすること
鉄則その2:輸液必要性があるのかを考えること
鉄則その3:輸液反応性があるかを考えること
鉄則その4:過剰輸液になっていないかを考えること
輸液必要性
このショックはSVが低下することによって起こっているものなのか?というのを判断し、もしSV低下が原因と判断したならば輸液をする、というステップを踏む必要があります。
ここで参考になるのは①乳酸値、②SvO2、③CO2ギャップ、④身体所見、の4つです。1つずつ解説していきますが、大事なのはこれらいずれの項目も「組織での酸素不足」を表す指標であることです。
乳酸値
酸素が末梢組織に十分に供給されていれば、グルコースを分解するときに好気性代謝が行われ、ATPを産生し、最終的にはH2OとCO2になります。この過程では乳酸は発生しません。
しかし酸素が十分に供給されていなければグルコース分解は嫌気性代謝となり、グルコース→ピルビン酸→乳酸、といった経路により乳酸が発生します。(思い出しただけでアレルギーが出そうな代謝経路については説明を省略します、、、)
つまり酸素が十分に供給されていれば乳酸値は上昇しませんが、酸素が不足している状態では乳酸値は上昇し得ます。
やや脱線しますが、例外として①代謝が亢進している状態(→敗血症など)、②NADH/NAD+比上昇(→アルコール摂取など)、③ビタミンB1不足、④ミトコンドリア機能異常(→敗血症など)、⑤クリアランス不足(→肝障害など)、では組織低酸素がなくても乳酸値は上昇します。
組織での低酸素があって乳酸が上昇することは多く、これをType Aの乳酸アシドーシスと呼び、組織での低酸素がなくて乳酸が上昇する場合をType Bの乳酸アシドーシスと呼びます。
SvO2
SvO2は静脈内の酸素飽和度のことです。通常酸素は、「動脈→組織→静脈」という経路で通過していくため、静脈内の酸素飽和度であるSvO2は組織で取り込まれたあとの残りの酸素を表しています。
SvO2の低下は①酸素供給が少ない、②酸素需要が大きく酸素消費が激しい、の2つの場合におこりますが、簡単にいえば酸素の需要供給が破綻したとき、拡大解釈すればショックの時、に起こるものと考えられます。
SvO2は肺動脈カテーテルでモニタリングした肺動脈の酸素飽和度をあらわしており、ScvO2は中心静脈から採取した血液(上大静脈)の酸素飽和度を表しております。2つの値は概ね相関するとされておりますが、ショックの時にはScvO2の方SvO2よりも5程度高い値になるといわれています。ScvO2≧70%、SvO2≧65%、が一つの基準となっています。
例外として以下の場合はSvO2が高値になってしまいますので、注意が必要です。
①組織が酸素を受け取らない場合:敗血症やシアン中毒により組織での酸素利用障害がある場合
②動脈血と静脈血のバイパスがある場合:透析シャント、心疾患などで左右シャントがある場合
CO2ギャップ
動脈血のPCO2と静脈血のPCO2の差で示される値です。つまり、
CO2ギャップ = PvCO2 – PaCO2
で表せます。
末梢組織で産生されたCO2は静脈血に乗って右心系まで運ばれ、肺に届き、肺で体外に放出されます。
体外に放出されたCO2の量をVCO2とすると、
VCO2 = CO × (CvCO2 – CaCO2) (※CvCO2:静脈CO2濃度、CaCO2:動脈CO2濃度)
となります。
濃度は分圧に比例するため、Kという比例定数を使うと、
VCO2 = CO × K × (PvCO2 – PaCO2)
⇔ (PvCO2 – PaCO2) = 1/k × VO2/CO
⇒ CO2ギャップ ∝ VCO2 /CO
が成立します。
つまり、COが低下するか、VCO2が上昇する(→代謝が亢進してCO2排出量が増える)、のいずれかによりCO2ギャップは増大します。
CO2ギャップが6mmHg以上であれば何らかの障害があると考えられています。
身体所見
shockを認知するために大事な身体所見として、「意識、尿量、皮膚」の「3つの窓」があります。
・意識:意識障害
・尿量:0.5mL/Kg/h以下の乏尿がある
・皮膚:mottling skin(網状皮斑)、末梢冷感、CRT延長、など
これらは組織低灌流の結果として表れる身体所見であるとともに、適切な輸液により改善する項目であり治療反応性をみるのにも有用です。(N Engl J Med. 2013; 369: 1726-34.)
まとめると、
・乳酸値上昇 ( ≧ 2mmol/L)
・SvO2低下 ( < 75%)
・CO2ギャップ増大 ( ≧6mmHg)
・3つの窓(意識、尿量、皮膚)の異常
があればCO低下、ひいてはSV低下によるショックが起こっている可能性があり、輸液必要性があると判断します。
いずれも例外になる場合が多く、「単一指標だけでは決めない」、という姿勢が重要です。
輸液反応性
輸液の必要性があったとしても、輸液が功を奏するかはまた別問題です。炎症が強く起こって血管透過性が亢進しきっているなんて場合には、血管内脱水に対して輸液をしても血管外に漏れ出るばかりで、輸液をしても改善は得られません。暖簾に腕押し状態です。。。
輸液をして改善するかの指標としてはいくつかあるのですが、静的指標と動的指標の2つに大別されます。
静的指標は輸液する前にチェックして輸液反応性をみる値であり、動的指標は実際に輸液をしてみる・輸液と近い状態を作る・呼吸による変動をみることにより反応性をみる値です。
静的指標にはCVPなどが、
動的指標にはfluid challenge、PLR(受動的下肢挙上テスト)、SVV、PPV、IVCの呼吸性変動、などがあります。
静的指標は様々な因子に影響を受けるためあまり鋭敏な指標ではなく、動的指標の方が輸液反応性の評価に向いているとされています。1つ1つ解説していきます。
CVP
静的指標として代表的なのがCVPですが、すでに有用性はないことが示されており、使用しません。
CVPによる輸液反応性の予測はある論文で「コイントスと同じ精度」と批判されています。(Chest. 2008; 134: 172-8.)
fluid challenge
4mL/Kgの晶質液を、5-10分間で輸液し、COが10%以上変化した、場合に輸液反応性あり、と評価できます。
4mL/Kgはだいたい200-250mLであり、このくらいであればもし輸液が失敗したとしても害になることは多くありません。
より厳密な管理をしたい(少しの失敗も許されない)場合には、
100mLの晶質液を、1分間で輸液し、COが5%以上変化した、場合に輸液反応性ありと評価する「mini-fluid challenge」というものもあり、こちらも有用です。
PLR
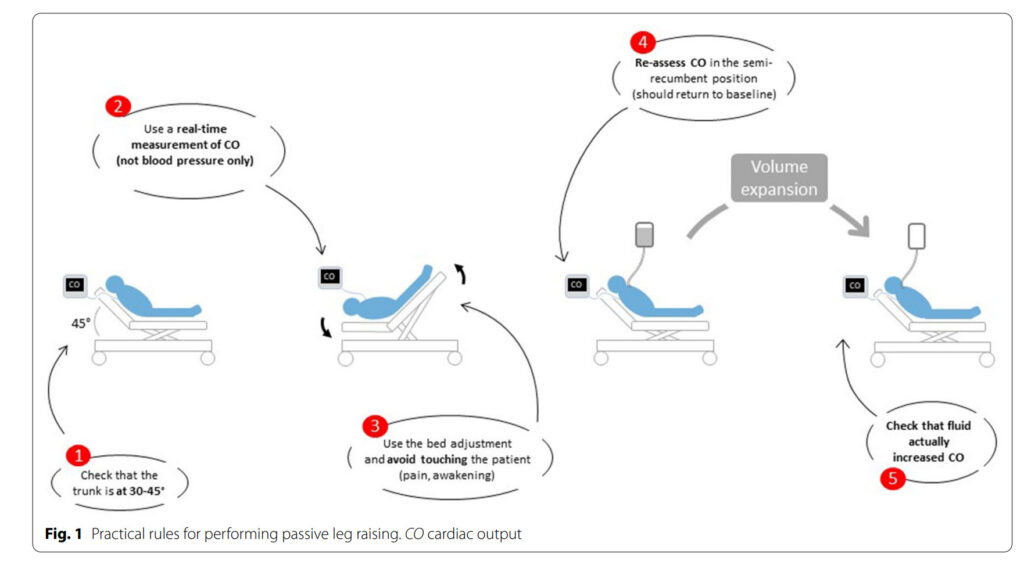
(Ann Intensive Care. 2022; 12: 46.)
Passive Leg Rising (受動的下肢挙上テスト)、のことです。
下肢を挙上することで300mL程度の血液が中枢に戻ってくるとされており、これによる反応性をみて輸液反応性を判断します。これのメリットは「実際に輸液をしないで済むこと」です。fluid challengeをしたいけど、そのせいで病態が悪化する危険があるな~という場合には特に有効です。治療域の狭い症例ではぜひ試したい手法ですが、方法に決まりがあるので覚えておく必要があります。
①45度ヘッドアップをした状態でCOを測定する
②ヘッドアップを解除し、下肢を挙上し、この状態でCOを測定する
③下肢挙上を解除し、再度45度ヘッドアップした状態に戻し、COを測定する
という手順です。
②で測定したCOが①で測定したCOよりも10%以上上昇した場合、輸液反応性があると判断します。
文献によりますが、あるMeta-analysisでは、感度89.4%、特異度91.5%で輸液反応性を予測できたという報告があります。
ここで重要なのは、ヘッドアップや下肢挙上はベッドのリクライニング機能のみを使用することであり、患者さんに触ってはいけないという点です。患者さんを刺激することにより、交感神経刺激が起こり、交絡因子が入ることを防ぐためです。その他、排痰が多ければテスト前になるべく吸引する、患者さんがawakeの場合にはテスト内容を説明し協力を仰ぐ、など交絡因子を少しでも排除する努力が必要です。
SVV・PPV
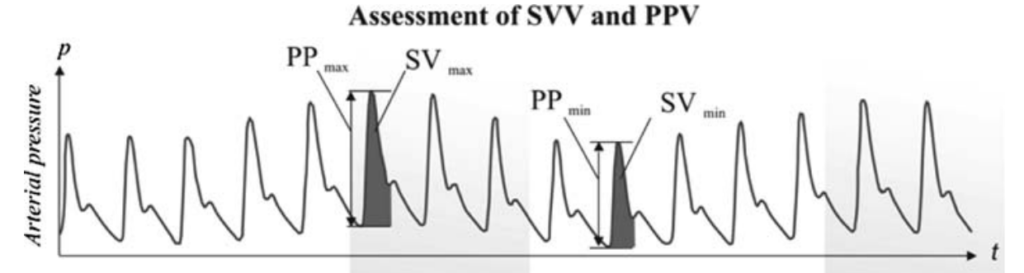
(J Clin Monit Comput. 2011; 25: 45-56.)
呼吸により静脈還流量や左室への後負荷が変化し、動脈圧の波形が変動します。この変動率を表したものがSVVとPPVです。
SVVとはStroke Volume Variation(一回拍出量変動)といい、動脈圧の曲線下面積から求めた一回拍出量の変化量をみる値です。PPVはPulse Pressure Variation(脈圧変動)は脈圧、すなわち収縮期血圧-拡張期血圧の変化量をみる値です。
いずれも12-13%以上あれば輸液反応性があると判断します。
しかし、不整脈、自発呼吸、低換気、などの条件下でないと正しく測定できないといわれており、使用する場面は限定されるかもしれません。(Ann Intensive Care. 2022; 12: 46.)
IVC呼吸性変動
IVCの測定については古典的によく用いられていた方法です。IVCの径ではなく呼吸性変動をみることが有用とされています。
IVC最大径をIVCmax、IVC最小径をIVCmin、とすると、
自発呼吸であれば「IVCmax – IVCmin / IVCmax」が40%以下、
人工呼吸であれば「IVCmax – IVCmin / IVCmin」が18%以下、
で輸液反応性があるとされております。(Ann Emerg Med. 2010; 55: 290-5., Intensive Care Med. 2004; 30: 1740-6,)
しかし報告によりますが感度特異度ともに71%との過去報告もあり、予測能が低く、かつ影響を受ける因子が多いことが問題点として指摘されており、あまり有用な指標でないのではないかと見直されつつあります。(J Intensive Care Med. 2020; 35: 354-63., Intensive Care Med. 2016; 42: 1164-7.)
過剰輸液
過剰輸液ではないか?という視点で、輸液する前にも、輸液する後にも確認する姿勢が重要です。
心不全の治療でも同様ですが、血行動態によるうっ血(LVEDPの上昇)は臨床的なうっ血(呼吸障害や全身浮腫などの所見)に先行すると言われており、なるべく血行動態によるうっ血を早期にピックアップして臨床的なうっ血に至るのを防ぐ、というのが大事なコンセプトです。
LVEDPは肺動脈カテーテルを使えばPAWPで評価ができますが、全例で肺動脈カテーテルを挿入するわけではないので、間接的な所見も抑えておく必要があります。評価項目として有用なのはエコー所見であり、①左室流入血流波形(TMF)、②IVC/VExUS、の2つの項目があります。
左室流入血流波形(TMF)
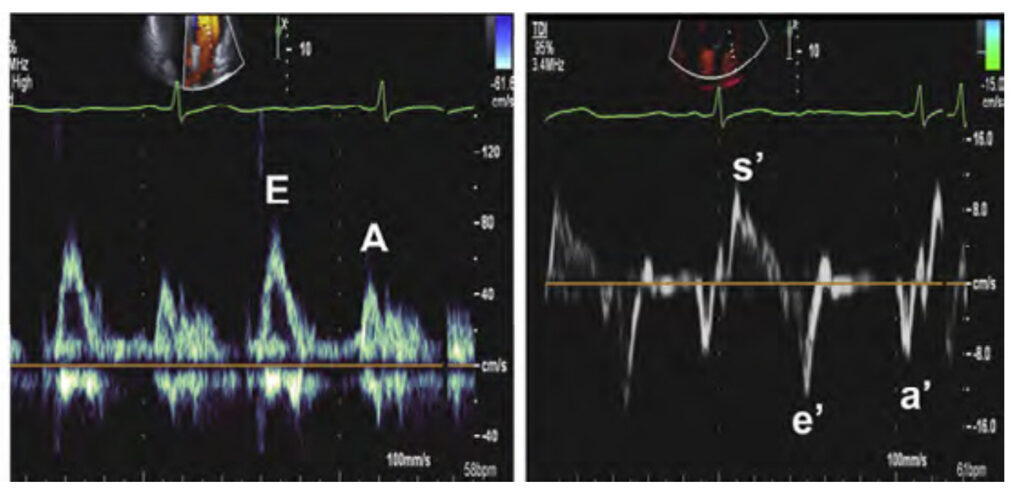
(J Am Soc Echocardiogra. 2016; 29: 277-314.)
詳しい当て方についてはまた別途ご紹介します。
主にE/A、E/e’、などを見ていきます。左房圧と拡張障害を推定するパラメータですが、過剰輸液によっても左房圧上昇は起こりうるため、参考になります。しかしやはり過剰輸液を直接的にみるものではないため、明確なカットオフ値というものはなく、連日評価してあくまでトレンドとしてみていくのがよいでしょう。
IVC/VExUS
従来、IVCを用いてCVPを予測してvolume overの可能性を予測するというやり方が行われていましたが、IVCに加えて肝静脈(HV)、門脈(PV)、腎臓内静脈(IRV)のエコー所見も加えた「VExUS grade」というものが最近注目されています。うっ血によるAKIの予測因子として優れると報告されております。
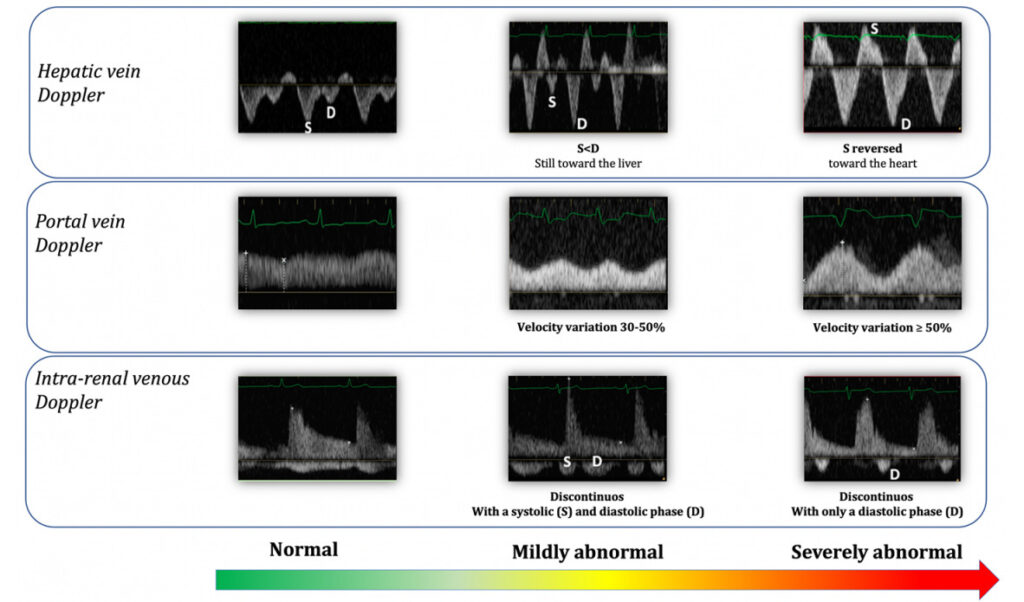
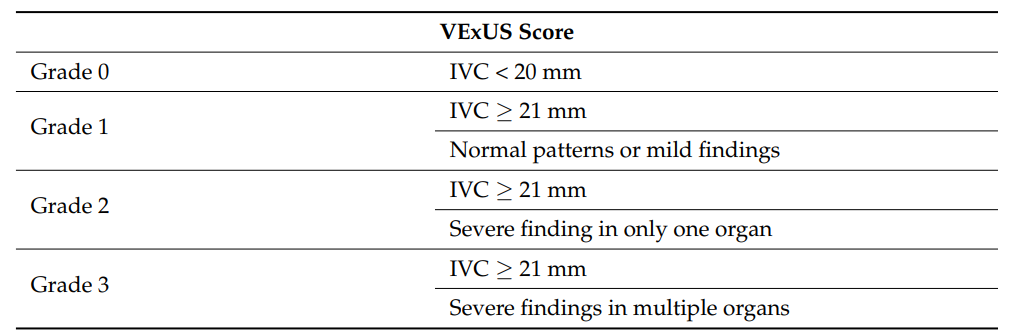
(J Clin Med. 2022; 11: 7538.)
ただし肝静脈はTRの影響を受ける、門脈は健康なアスリートでも軽度拡張が見られる、腎臓内静脈はそもそも描出が難しい症例がある、などの制限があるのは認識しておく必要があります。(Ultrasound J. 2021; 13: 32.)
さいごに
輸液必要性と輸液反応性に分類して評価していく姿勢が重要です。
そしてつねに過剰輸液にならないか?という視点も持っておきましょう。
PLRだったりエコーだったり、症例全てに毎回繰り返しやるのはさすがに非現実的ですが、、、治療域の狭い重症症例や、輸液しても思ったような結果が出ないとき、などはきちんと評価するべきです。